Protein supplementation improves physical activity in frail elderly subjects: randomized, double-blinded, placebo-controlled trials.
作者:陳曦
所屬單位:保健營養學系四年級
< 前言 >
衰弱症 (frailty) 是指在健康是易受傷害的傾向和多種身體系統失去功能的進程;常用 Fried criteria 作為檢測標準,內容包括:非自願性體重流失、肌肉無力、疲勞、行走速度緩慢和低身體活動度,衰弱會增加跌倒、失能、住院以及死亡的可能;據衛生福利部國民健康署2017年報的資料,台灣老年人口處於亞健康和衰弱前期有 20 %,衰弱症則有 10 %,預防和減緩衰弱症的發生是重要的課題。
肌少症 (Sarcopenia) 是衰弱症發生的一大原因,肌少症與衰弱症共同的危險因子包含:低身體活動度和蛋白質攝取不足,因肌少症與衰弱症是惡性循環的關係,維持老年人健康必須同時著重避免衰弱症和肌少症的發生;但目前對於老年人蛋白質的補充影響肌肉量和體能表現上的研究還沒有一致的結果。
< 研究主題與目的 >
在於探討衰弱老年族群攝取多少量的蛋白質有助於延緩衰弱症發展。
< Paper 1 > Protein supplementation improves muscle mass and physical performance in undernourished prefrail and frail elderly subjects: a randomized, double-blind, placebo-controlled trial. Park Y, Cho JE, and Hwang HS. Am J Clin Nutr; 108: 1026– 1033 (2018)
一. 材料與方法
(一) 研究設計
- 12 週的隨機、雙盲、安慰劑控制、三平行組並使用分組隱匿 (Concealed allocation) 和意象分析 (Intention-To-Treat analysis, ITT) 的臨床試驗。
- 在實驗開始前有一次為期四週的檢測拜訪,內容包含:收集心血管健康研究(Cardiovascular Health Study, CHS) 衰弱症指標、迷你營養評估 (Mini nutritional assessment, MNA)、背景資料、醫療資訊、身體質量指數 (Body Mass Index, BMI) 和三天飲食紀錄等資料。
- 第 0 週、第 6 週和第 12 週各有一次拜訪,會收集醫療就診紀錄、南韓健康縱向研究(South Korean Longitudinal Study on Health and Aging, KLoSHA) 的衰弱症指標、計時起走測驗(Timed up-and-go test, TUG test),還有血液、尿液樣本並發放介入的蛋白質或安慰劑粉末。
- 第 0 週和第 12 週額外測量肌肉量和執行 MNA 檢測。
- 介入期間每兩週會進行一次三天飲食紀錄和收集副作用的回饋。
(二) 受試者
- 受試者為 120 位年齡介於 70 至 85 歲,且被定義為衰弱症前期或衰弱症與有營養不良的風險的老年人。
- 排除條件:患有肝功能或腎功能衰竭、參與其他臨床試驗、無法行走或溝通、不符合衰弱症指標、MNA分數 > 23.5 的高齡者。
(三) 實驗介入
- 受試者隨機分配到三組,分別是蛋白質攝取 0.8 g/kg/d、1.2 g/kg/d 和 1.5 g/kg/d,由獨立的外部研究者操作電腦軟體進行隨機分配。
- 受試者被要求維持平常的飲食型態和運動習慣。
- 根據飲食紀錄發放蛋白質和安慰劑粉末使每位參與者達到蛋白質目標攝取量。
- 每位受試者會得到一天五包 10 公克的蛋白質或安慰劑粉末,蛋白質粉末含有脂肪 0.5 克、可可粉 0.2 克、乳清蛋白 9.3 克;安慰劑粉末含有脂肪 0.5 克、可可粉 0.2 克和麥芽糊精 9.3 克;介入或安慰劑可提供每天兩百大卡的熱量。
(四) 結果測量方法
- 雙能 X 光吸光測定儀 (Dual- energy X-ray absorptiometry, DXA) 測量四肢肌肉量 (Appendicular Skeletal Muscle mass, ASM) 以計算四種骨骼肌肉量指數 (Skeletal Muscle mass Index, SMI),包括以 ASM 校正身高、體重、BMI、體脂肪後的數值。
- 空腹的血液樣本測量尿素氮 (Blood Urea Nitrogen, BUN) 等項目,對尿液進行檢驗。
- 衰弱症使用 CHS frailty criteria 和 KLoSHA frailty criteria 檢定。
CHS frailty criteria 以下五項符合三項以上即可定義衰弱症之存在。
●疲勞感:使用流行病學研究中心的憂鬱症量表 (Center of Epidemiological Studies Depression scale, CES-D scale) 定義。
●低身體活動度:以國際身體活動問卷計算參與者一週的運動情形。
●行走速度緩慢:三次的四公尺行走速度平均值≤ 0.8m/s。
●非自願性體重流失:與去年體中比較下降 ≥ 4.5kg,定義為非自願性體重流失。
●肌肉無力:使用握力計測量參與者站姿雙手各兩次的握力。
KLoSHA frailty criteria
由簡短身體功能量表 (Short Physical Performance Battery, SPPB) 、韓國日常活動分數、韓國迷你精神狀態檢測分數 (Korean Mini Mental State Examination, K-MMSE) 和血清白蛋白濃度所組成。 - 以 MNA 檢測受試者是否有營養不良的風險。
(五) 統計分析
- 使用 PROC MI 檢定分析數據組,利用 PROC MIANALYZE 檢定探討結果的關係。
- ANOVA 用來確認沒有選擇性偏誤,類別變項使用 chi-square 和 Fisher’s exact test 分析,ANCOVA 分析 ASM、SMI、飲食狀態之間的關係,以混合線性模型分析體能表現和安全性。
- 所有統計皆使用 Statistics Analysis System 9.4 進行分析。
二. 結果
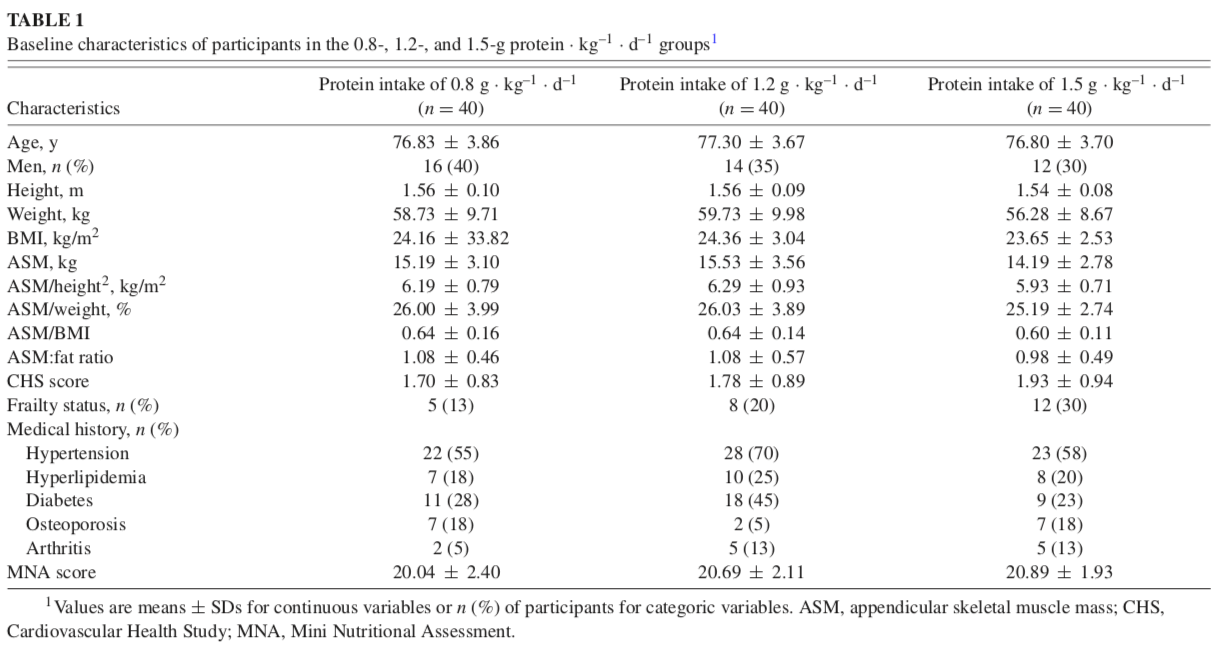
- 本研究三組在 baseline 的數據皆沒有顯著差異。(Table 1)
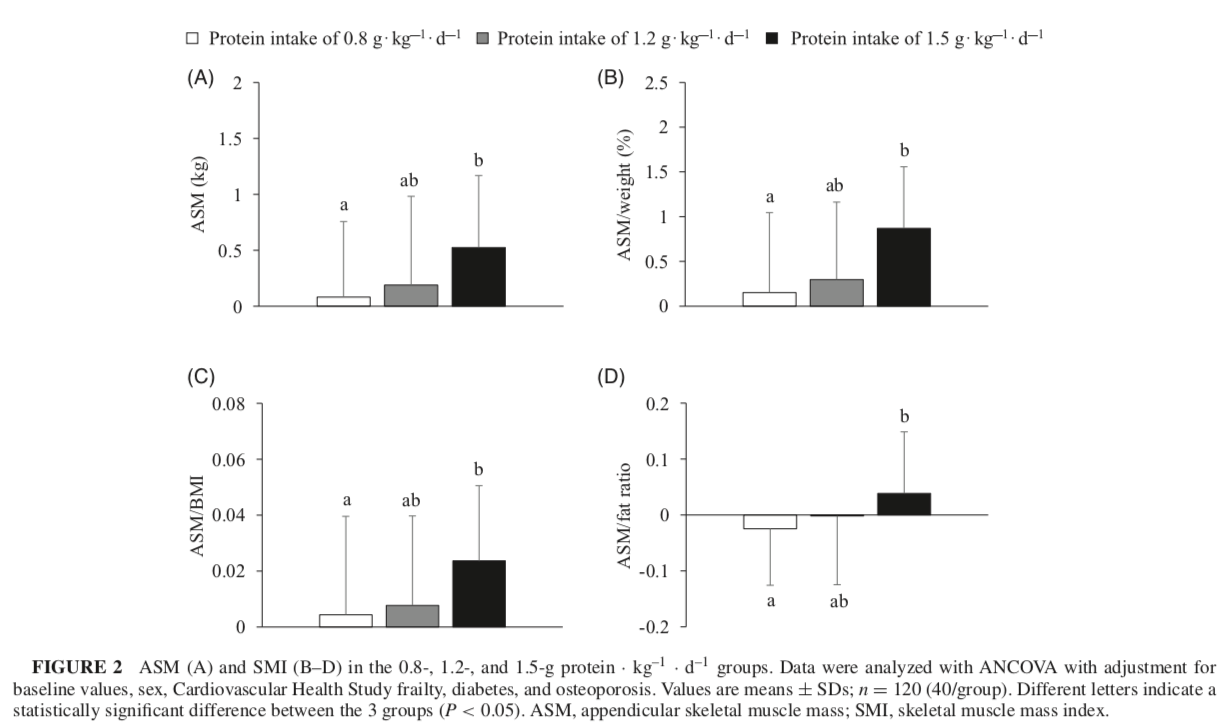
- 蛋白質攝取 1.5 g/kg/d 組的 SMI 顯著大於 0.8 g/kg/d 組,但 1.2 g/kg/d 組和另外兩組沒有顯著差異。(Figure 2)
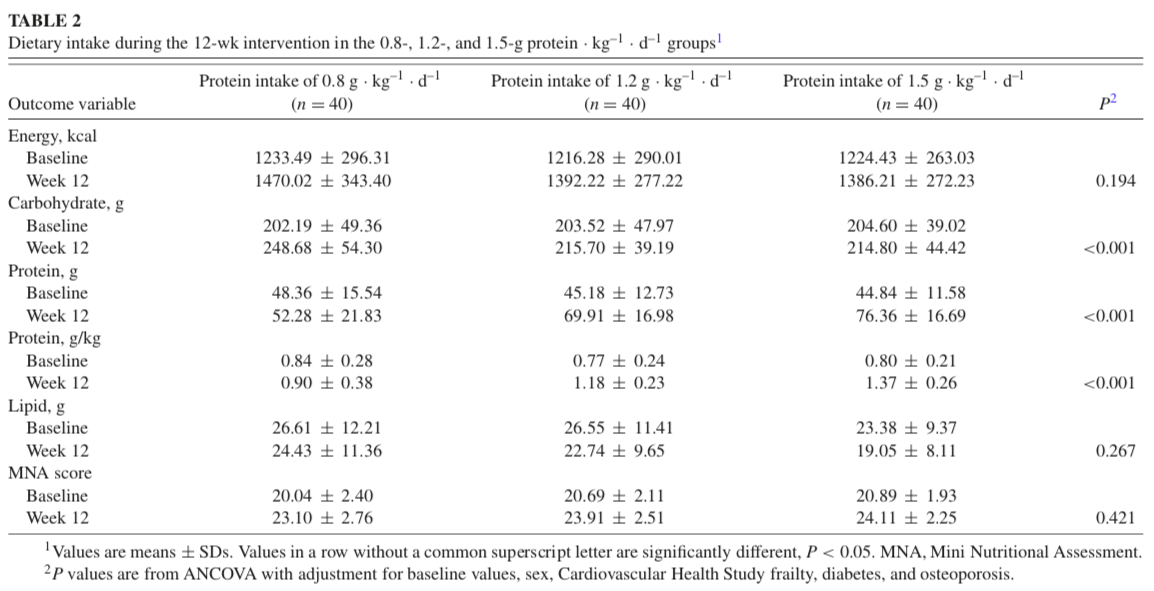
- 飲食中蛋白質攝取量 1.5 g/kg/d 組顯著大於另外兩組,而醣類攝取量則是 0.8 g/kg/d 組顯著最高。(Table 2)
- 經過 12 週的介入,1.5 g/kg/d 組相較其他兩組有顯著較快的行走速度,而兩種衰弱症分數、SPPB、平衡測驗、坐姿站立、K-MMSE、TUG test、握力只有在時間上有顯著差異,並沒有組間差異。(Table 3)
三. 討論
- 本研究顯示蛋白質攝取量 1.5 g/kg/d 可改善受試者的 ASM、SMI、行走速度,但發現蛋白質攝取量與肌肉量並沒有劑量反應關係。
- 乳清蛋白含有大量的 Leucine 可以促進蛋白質的活化來調節肌肉蛋白質的生成,是最適合進行蛋白質生合成的蛋白質,也是本篇作者選用乳清蛋白介入的原因。
- 與平常蛋白質攝取量的差距會影響肌肉的合成,先前的研究發現與平常攝取量 0.4 g/kg/d 的差距是促進肌肉生長的臨界值,這就能解釋 1.2 g/kg/d 組沒有增加 SMI 的原因。
- 本研究的受試者在體能表現上有所進展,並且發現在肌肉有可測量的改變前就可觀察到身體功能上的改善,與先前研究一致。
- 作者歸納出:功能衰弱與熱量、蛋白質的攝取量相關,並觀察到此次介入沒有造成副作用。
- 研究優勢:受試者精準反映有營養不良的衰弱前期或衰弱症老年族群,且三組有類似的baseline 資料;飲食攝取和遵從度由營養師監測搭配重複的 24-h 回憶法驗證。
- 研究限制:受試者可能逐漸熟悉重複的測驗流程、沒有控制介入的時間點、可能因分析多項結果的變異而造成 type I error。
四. 結論
有營養不良風險的衰弱前期或衰弱老年人攝取1.5 g/kg/d的乳清蛋白改善肌肉量和體能表現。
< Paper 2 > Protein supplementation improves physical performance in frail elderly people: a randomized, double-blind, placebo-controlled trial. Tieland M, Rest O, Dirks M, Zwaluw N, Mensink M, Loon L, Groot L. JAMDA; 13: 720– 726 (2012)
一. 材料與方法
(一) 研究設計
- 受試者由外部研究者利用電腦軟體隨機分組到蛋白質介入組或安慰劑組。
- 介入期間的第 0 週、第 12 週和第 24 週會收集所有的測量值。
- 肌肉量利用 DXA 測量,橫切面的肌肉纖維使用肌肉切片觀察。
- 力量以一次反覆最大重量肌力 (1 repetition maximum, 1- RM) 和握力檢測,以SPPB 測量體能表現。
- 空腹時會測量血液樣本,包括測量血糖、胰島素和腎功能指標,還有檢測血壓。
- 營養師執行三天飲食紀錄來調查受試者平常的飲食型態。
- 健康狀態使用 12 項目的簡短健康調查 (12-item Short Form Health Survey, SF-12) 檢測,認知功能以迷你精神狀態檢測 (Mini Mental State Examination, MMSE) 調查。
(二) 受試者
- 受試者 65 位年齡為 65 歲以上的老年人,且在兩年內沒有參與任何運動訓練計畫。
- 排除條件:罹患癌症或慢性阻塞性肺病、血糖 > 7 mmol/L、eGFR < 60 ml/min/1.73 m2。
- 獨立外部研究者操作電腦軟體進行隨機分配並分派受試者新的識別證。
(三) 實驗介入
- 介入時間為每天早餐和午餐後各飲用一瓶介入飲品。
- 受試者會得到每瓶 250 毫升的介入或安慰劑飲料,介入物含有蛋白質 15 克、乳糖 7.1 克、脂肪 0.5 克和鈣 0.4 克;安慰劑不含蛋白質,有乳糖 7.1 克和鈣 0.4 克。
(四) 統計分析
- 根據 ITT 原則和先前已經設計好的數據分析計畫執行統計分析。
- baseline 數據使用獨立 student’s t-test 分析
- 數據間的差異利用混合線性模型搭配 Toeplitze 共變結構檢測,肌肉量是前述方法再加入受試者內因子分析。
- 所有統計皆使用 SPSS 19.0 進行分析。
二. 結果
- 受試者在第 0 週數據皆沒有顯著差異,且兩組在 MMSE 分數都超過 25 分,代表沒有認知障礙。(Table 1)
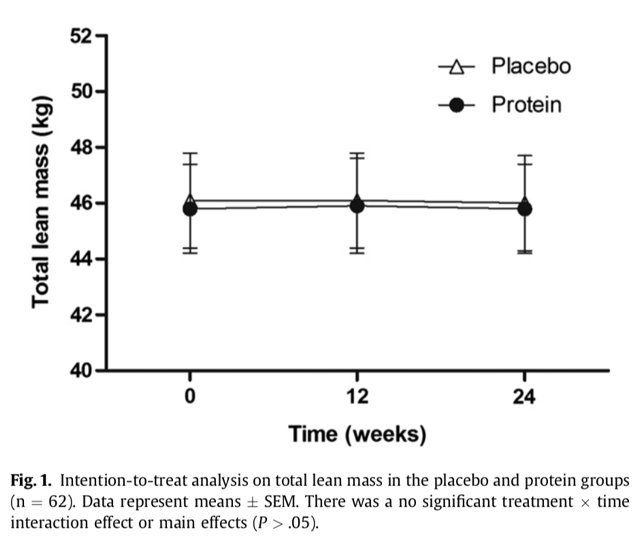
- 第 0 週、第 12 週和第 24 週,身體組成數據皆沒有顯著差異。(Table 2、Figure 1)
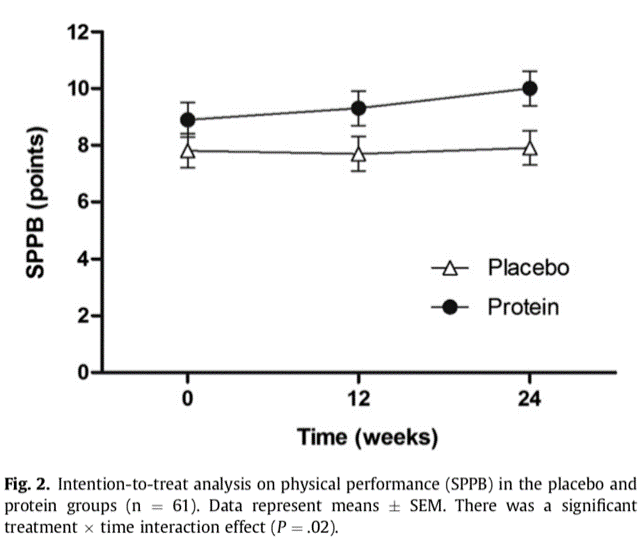
- 兩組的肌肉量和 SPPB 分數在第 0 週沒有顯著差異,腿伸屈的部分有組間和時間上改善的趨勢;隨時間的改變,蛋白質組的 SPPB 分數有顯著提升,且在坐姿起立有最明顯的差異。(Table 3、Figure 2)
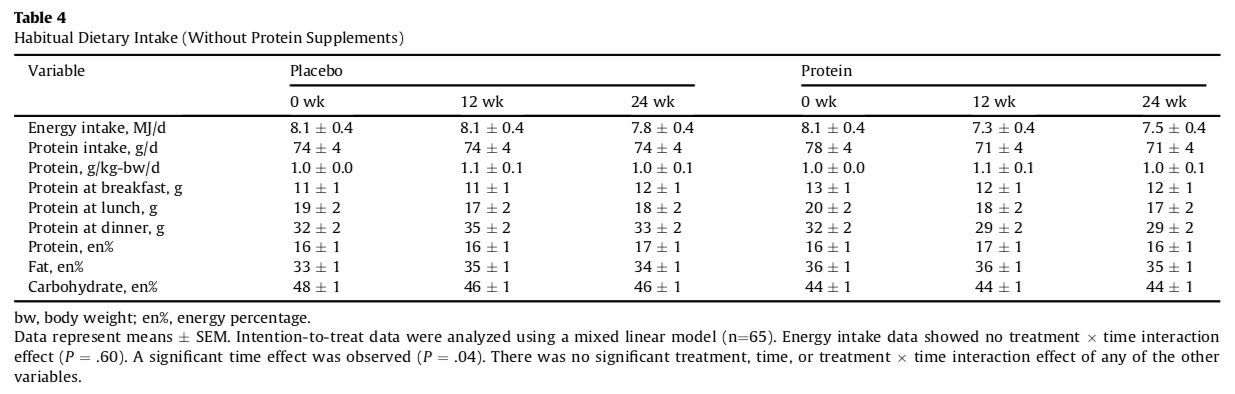
- 兩組的飲食蛋白質攝取在第 0 週是 1.0 g/kg/d,介入期間也沒有改變,加上每天 30 克的蛋白質補充後,蛋白質組蛋白質的攝取量為 1.4 g/kg/d;經過 24 週的介入,蛋白質組的熱量攝取顯著下降,安慰劑組持平。(Table 4)
三. 討論
- 本研究顯示 24 週的飲食蛋白質補充無法增加衰弱老年人的肌肉量,但可提升體能表現。
- 與先前研究一致,本篇研究受試者在 baseline 三餐蛋白質攝取量分配不均,介入後,三餐的蛋白質攝取量皆大於 25 公克,可促進餐後肌肉蛋白質的合成。
- 本研究介入後,並沒有增加受試者的肌肉量,雖然小於 1 公斤的肌肉增長是無法測量的,但作者認為長遠來看還是有臨床上的益處。
- 體能表現在蛋白質組有顯著的進步,SPPB 分數顯著提升,作者觀察到在肌肉量有可測量的成長之前,會先觀察到力量或體能表現的改善。
- 本篇的介入讓蛋白質攝取增加到 1.4 g/kg/d 並沒有發生副作用,因此,蛋白質補充在衰弱老年人的應用可改善體能表現、減緩衰弱症發展和延緩失能的發生,是可信的營養策略。
四. 結論
每天兩次,每15 克的長期蛋白質補充可改善衰弱老年人體能表現,但無法增加肌肉量。
< 總結 >
攝取每天1.4 g/kg的蛋白質可以有效改善衰弱症老年人的體能表現,並減緩衰弱症的發展。
五. 參考文獻
Hwang SH, Kwon IS, Park BJ, Cho B, Yoon JL, Chang WW (2010) The Validity and Reliability of Korean Frailty Index. J Korean Geriatr Soc 14 (4) 191- 202.